12:38 Биологические свойства пробиотиков | |
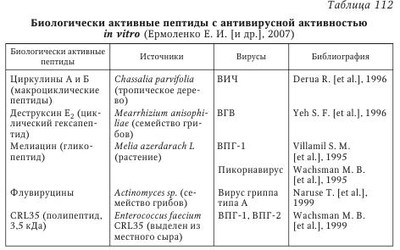
Известно участие иммуномикроэкологической системы человека в поддержании его здоровья и снижении риска развития заболеваний. Нарушения в иммунном и микроэкологическом статусе человека имеют важное, а порой и определяющее значение при традиционных инфекционных заболеваниях и в этиопатогенезе многих новых, так называемых «болезней цивилизации». Можно сказать, что любая патология внутренних органов сопровождается изменениями кишечного микробиоценоза. В свою очередь, сопутствующие дисбиотические изменения кишечника, достигающие определенного уровня, ухудшают клиническое течение основного заболевания. Важно, что если в ходе лечения не удалось добиться оптимизации состояния кишечного микробиоценоза, чаще наступают рецидивы и варианты осложненного течения основного заболевания. Важной причиной развития воспаления в патогенезе различных инфекционных и соматических заболеваний является эндотоксемия, связанная с дисбиозом кишечника. Предполагается, что развитие эндотоксемии при неалкогольном стеатогепатите характеризуется, с одной стороны, повышенной выработкой таких провоспалительных цитокинов, как фактор развития некроза опухоли а (ФНО-а), ИЛ-6 и ИЛ-8, а с другой — повышенной экспрессией рецепторов к провоспалительным цитокинам. Микробиоценоз кишечника, являясь открытым, соприкасающимся с внешней средой, может испытывать постоянные воздействия, которые приводят к изменениям состава микробиоты. Различные факторы — характер питания, воздействие ксенобиотиков, лекарств, состав воды, усталость, изменение климата, физические и психические перегрузки могут приводить к непродолжительным изменениям состава кишечной микрофлоры (дисбиотическая реакция) или изменению качественного и количественного ее состава, т. е. дисбиозу. Поддержание микробиологического постоянства внутренней среды кишечника осуществляется благодаря содружественной работе иммунной и пищеварительной систем, поэтому нарушения их деятельности приводят к стойким нарушениям биоценоза. Существуют различные способы поддержания и восстановления кишечной эндоэкологии, что достаточно полно изложено в соответствующей литературе. Хороший эффект получен при лечении дисбиоза кишечника пробиотиками, пребиотиками, симбиотиками и синбиотиками. Пробиотики — это живые микроорганизмы и вещества микробного и иного происхождения, оказывающие при естественном способе введения благоприятные эффекты на физиологические функции, биохимические и поведенческие реакции организма хозяина через оптимизацию его микроэкологического статуса. Под оптимизацией экологического статуса следует понимать и борьбу с патогенными бактериями, простейшими, грибами и, как показано в последние годы, вирусами. Наиболее распространенным являлось применение лиофилизированных живых или убитых штаммов бактерий — представителей нормальной микрофлоры (бифидобактерий, лактобацилл, кишечной палочки). Выделяют пять групп пробиотических препаратов в зависимости от количества содержащихся в них штаммов микроорганизмов: 1-я группа — монокомпонентные препараты (бифидумбактерин, лактобактерин, колибактерин, нормофлор, ромакол, наринэ и др.). Они состоят из одного микроорганизма, являющегося типичным обитателем кишечника. 2-я группа — препараты конкурентного действия, вытесняющие условно-патогенные и патогенные микробы и в дальнейшем не колонизирующие кишечник. К ним относят нетипичных обитателей кишечника: бактерий рода Bacillus subtilis (бактисубтил, биоспорин и др.) и дрожжи — Saccharomyces boulardii (энтерол). 3-я группа — поликомпонентные препараты, или симбиотики. Они состоят из нескольких штаммов бактерий одного и того же рода и вида (ацилакт, витафлор, лактофлор и др.) или из нескольких бактерий различных групп и семейств (бифацид, бифидин, линекс, би-фитон, бификол и др.). 4-я группа — комбинированные препараты, или синбиотики, которые содержат бактерии и специальные ингредиенты, способствующие их росту и/или размножению, и/или метаболической активности (бифилиз, аципол, кипацид, биовестин-лакто, нутролин В и др.). 5-я группа — поликомпонентные комбинированные препараты (бифиформ, ламинолакт). В состав бифиформа входят 2 вида бактерий (бифидобактерии, энтерококки) и специальные ингредиенты, способствующие их росту, размножению, метаболической активности. Препараты данной группы являются одновременно и симбиотиками, и синбиотиками. Большинство современных пробиотических препаратов и продуктов включают в себя так называемые «молочнокислые бактерии» — lactic acid bacteria (LAB). LAB — репрезентативная группа бактерий (Lactobacillus spp., Enterococcus spp., Streptococcus spp., Lactococcus spp., Leuconostoc spp.), которые связывают способность продуцировать молочную кислоту как единственный продукт (гомофер-ментативный метаболизм) или молочную кислоту вместе с другими продуктами (гетероферментативный метаболизм). LAB разрушают глюкозу с образованием молочной, уксусной кислот, этанола и углекислого газа, некоторые из них продуцируют перекись водорода. Кроме действия на бактерии, грибы и простейшие, пробиотические препараты оказывают и противовирусный эффект. Показано, что лактобактерии предотвращают или облегчают течение инфекций, вызванных ротавирусами, цитомегаловирусами, вирусами гриппа и вирусами иммунодефицита человека. Эти эффекты были установлены на основании клинических наблюдений и объяснены стимуляцией иммунной системы. На экспериментальной модели была показана способность молочнокислых бактерий индуцировать синтез специфических IgA, стимулировать репарацию повреждений энтероцитов и увеличивать активность NK-клеток. Был продемонстрирован также прямой противовирусный эффект LAB, связанный с продукцией H2O2 или продукцией молочной кислоты. Добавляя различные факторы при культивировании вирусов в культуре клеток, была показана способность пептидов растительного и микробного происхождения оказывать вирусостатическое и вирулицидное действие (табл. 112). Наиболее интересные данные касаются энтероцина, выделенного из пробиотического штамма Enterococcus faecium CRL35, способного ингибировать репродукцию ВПГ-1, ингибируя синтез гликопротеида D, компонента суперкапсида вируса. Однако использование пробиотиков у больных с дисбиотическими нарушениями имеет свои ограничения, а в ряде случаев способствует обострению заболевания. Это обусловлено низкой способностью введенных извне лиофилизированных микроорганизмов к выживанию в кишечнике, созданию ими дополнительной антигенной нагрузки и нежелательной сенсибилизации организма, а также тем обстоятельством, что дисбактериоз кишечника редко имеет изолированный характер. Указанные обстоятельства вызвали внедрение в клиническую практику неферментируемых в кишечнике пищевых добавок, способных к селективной стимуляции роста и активности прежде всего собственных бифидо- и лактобактерий — пребиотиков. Важное значение имеет способ введения и стратегия использования пробиотического препарата и продукта, которые должны учитывать особенности антимикробной активности и иммуномодулирующего эффекта этих терапевтических средств. Взаимоотношения молочнокислых бактерий с другими микроорганизмами зависят от условий среды обитания и могут изменяться в процессе развития микроорганизмов. Общеизвестно, что антибактериальная микробная активность LAB связана с конкуренцией за рецепторы и метаболиты, с продукцией перекиси водорода и оксида азота, органических кислот, бактериоцинов и бактериоциноподобных субстанций, с изменением pH среды в сторону увеличения кислотности. Таким образом, целесообразность использования про- и пребиотических препаратов и продуктов в терапии бактериальных и вирусных инфекций подтверждается несколькими основными положениями: 1. Многие инфекционные заболевания часто регистрируются как смешанная вирусно-бактериальная патология. Антибактериальная, противовирусная терапия, средства для лечения протозойной и кандидозной инфекций способствуют развитию дисбиотических состояний, в связи с чем показано применение про- и пребиотиков. 2. Инфекции, как правило, сопровождаются развитием вторичной иммунологической недостаточности, на фоне которой наблюдается дисбаланс в составе микрофлоры кишечника и влагалища. Использование пробиотических препаратов оказывает иммуномодулирующий и антимикробный эффекты на системном и местном уровнях макроорганизма. 3. Как показано в экспериментах in vitro, пробиотические культуры и продукты, продуцируемые ими в окружающую среду, могут оказывать губительное воздействие на микробные клетки, вирусные частицы и их репродукцию. | |
|
| |
| Всего комментариев: 0 | |