11:32 Эффективность системной энзимотерапии в лечении опоясывающего герпеса | |
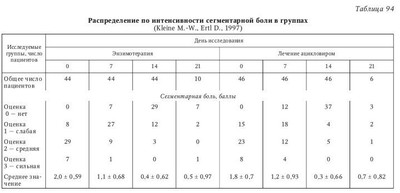
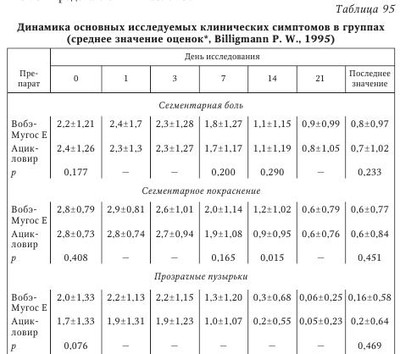
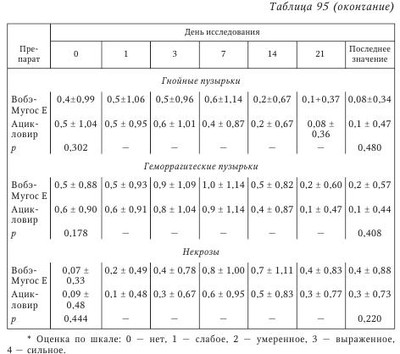
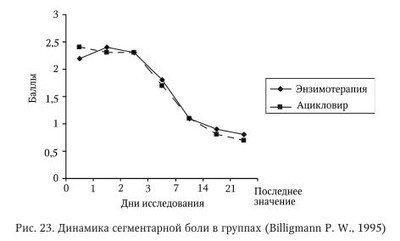
Опоясывающий герпес (ОГ) остается серьезной медицинской и социальной проблемой. Это связано как с широким распространением заболевания, так и с высокой частотой формирования отдаленных последствий, в частности синдрома постзостерной невралгии (ПЗН), ухудшающего качество жизни пациентов. При реактивации вируса варицелла-зостер (ВВЗ), оставшегося в латентном состоянии в спинальных ганглиях после первичного заболевания ветряной оспой, развиваются характерная сыпь и болевой синдром. Чаще ОГ проявляется у людей с признаками вторичной иммунологической недостаточности (ВИН), вследствие чего ослабевает иммунологический контроль ВВЗ, который находится в латентном состоянии. Исследования, проведенные в различных возрастных группах, показали, что решающую роль в подавлении вируса играют иммунологические механизмы. Оптимальная терапия ОГ должна, в первую очередь, снижать или устранять сегментарную боль, подавлять или блокировать репликацию вируса, ограничивать распространение проявлений болезни и обеспечивать репарацию имеющихся поражений кожи, в частности пузырьков и корочек. He менее важно и предотвращение отдаленных последствий или отсроченных осложнений, уменьшение проявлений ПЗН. Для лечения ОГ широко применяется АЦ в дозировке 800 мг 5 раз в сутки. Его угнетающее действие на репликацию ВВЗ, сегментарную боль и изменения кожи было показано во многих исследованиях. Ho вместе с тем известны побочные эффекты лечения и ограничение его у пациентов с заболеваниями печени и почек, существенно ограничивающие его применение. Считают, что лечение ОГ и ПЗН в целом находится на уровне ниже удовлетворительного. Альтернативным методом лечения ОГ можно считать метод СЭТ, сопоставимый по эффективности с лечением АЦ. Возможности полиэнзимной (системной) энзимотерапии в лечении аутоиммунных, воспалительных и иммуновоспалительных заболеваний, доказанные механизмы действия широко освещены в литературе. Значительный интерес представляют возможности энзимов в лечении и профилактике ГВИ, что продиктовано базовыми возможностями метода оказывать полимодальный, неспецифический эффект — комплексное влияние на иммунную систему (активация иммуноцитов, нормализация уровня цитокинов, разрушение и выведение иммунных комплексов, нормализация интерферонового статуса), влияние на механизмы воспалительной реакции. Описано использование препаратов СЭТ (Вобэнзим, Флогэнзим) при первичном заражении ВПГ во время беременности, при реактивации ГВИ во время беременности, ГГ. Приведем обобщенные данные по эффективности и переносимости препарата СЭТ — Вобэ-Мугос E в лечении ОГ. Вобэ-Мугос E (Мукос Фарма, Германия, регистрационный номер в России П № 015522/01) имеет в своем составе химотрипсин 40 мг (200 мккат), трипсин 40 мг (29 мккат) и папаин 100 мг (270 F. I. Р. Е) и относится к препаратам СЭТ с преимущественным иммуномодулирующим и противовирусным действием. В литературе описаны эффекты Вобэ-Мугос E как адъювантной (сопроводительной) терапии при лечении рака, помогающей свести к минимуму побочные эффекты лучевой и химиотерапии, тяжелые осложнения, улучшить течение фатальных стадий. В работе М. Wald показана способность Вобэ-Мугос E предотвращать и ингибировать развитие опухоли и метастазов меланомы В-16 у экспериментальных животных. Первые результаты использования препарата Вобэ-Мугос E в лечении 43 пациентов с ОГ были оценены как обнадеживающие: заметно быстрее, чем с помощью использовавшихся ранее комбинаций медикаментов, купировались симптомы ОГ. Первая попытка сравнить эффективность протеолитических ферментов и стандартно применяемого при лечении ОГ ацикловира была предпринята в рамках рандомизированного исследования в параллельных группах, проведенного с участием 20 пациентов. Так, 10 пациентов получали 5 раз в сутки по 4 испытательные капсулы Вобэ-Мугос E (что соответствует приему 5 раз в сутки по 3 таблетки), другие 10 пациентов получали 5 раз в сутки по 4 испытательные капсулы АЦ (800 мг АЦ). Лечение проводили до исчезновения всех симптомов, но не менее 2 нед. Использование других лекарственных препаратов, способных повлиять на течение ОГ, было запрещено. Прием анальгетиков разрешался, но отмечался в историях болезни. Исходные данные пациентов по возрасту, полу, росту, весу, основному заболеванию и симптоматике были сопоставимы. При контрольном обследовании на 7-й и 14-й день лечения для главных критериев — сегментарного покраснения и сегментарной боли — не было обнаружено статистически достоверных различий между группами (р > 0,05). При этом для боли удалось рассчитать избирательность («мощность»), равную 72 % (в = 0,28), а для покраснения — 67 % (в = 0,33). Несмотря на то что количество пациентов слишком мало для окончательного заключения, при статистических расчетах были выявлены определенные тенденции. В группе, получавшей ферменты, среднее значение оценки эффективности, сделанной врачом, было равно 2,4 (между «хорошо» и «удовлетворительно»). В группе, получавшей АЦ, среднее значение было равно 2,3 (между «хорошо» и «удовлетворительно»). Группы не различались между собой (р = 1,000). Эффективность лечения была оценена пациентами аналогично — в среднем как «хорошая» — 2,1 балла при приеме энзимов и 2,0 балла при приеме АЦ. Группы статистически не различались (р = 1,000). Данные предварительного исследования оказались аналогичны результатам, полученным М.W. Kleine в многоцентровом рандомизированном проспективном двойном слепом исследовании в параллельных группах, где изучалась эффективность и переносимость Вобэ-Мугос E и АЦ у больных ОГ. Исследование выполнено согласно пересмотренной Хельсинкской декларации, Германского фармацевтического закона (AMG) и принципов GCP. В 8 исследовательских центрах наблюдались 98 амбулаторных пациентов с ОГ, которых случайным образом распределили на две группы (планирование блоков методом случайных перестановок, размер блока 4), получавшие различное лечение — полиферментный препарат Вобэ-Мугос E или АЦ. Пациенты были в возрасте от 18 до 80 лет, диагноз ОГ установлен клинически по наличию сегментарной боли, сегментарной эритемы и везикул, при этом пациенты соблюдали запланированную дозировку и ежедневно вели дневник. Критериями исключения являлись: возникновение первых пузырьков ОГ более чем за 96 ч (четыре дня) до начала лечения; первое появление везикул более чем за 48 ч до включения в исследование; генерализованная герпес-зостерная инфекция; ранее проведенное лечение ОГ; непереносимость любого из компонентов исследуемых препаратов (лидокаина или клиохинола); беременность; кормление грудью; отсутствие информированного согласия; почечная недостаточность (клиренс креатинина < 10 мл/мин или креатинин в сыворотке > 6 мг/100 мл). Длительность наблюдения за каждым пациентом составила 14 дней, но при сохранении везикул или корочек продолжалось до 21 дня, когда происходило последнее контрольное обследование. В сутки включения в исследование (день 0) собирали предусмотренные протоколом антропометрические и анамнестические данные. Лекарственную терапию начинали в сутки 0 с инъекции содержимого ампулы с исследуемым веществом (комбинация ферментов или плацебо), растворенным в ампуле носителя (лидокаин) — энзимная группа получала инъекцию Вобэ-Мугос Е; группа, принимавшая АЦ, получала инъекцию плацебо. Затем с дня 0 по день 7 пациенты получали per os 5 капсул исследуемого вещества 4 раза в сутки. Было разрешено дополнительное наружное применение лосьона, содержащего 0,5 % клиохинола, который наносили местно 1 раз в сутки; в случаях острой боли разрешалось лечение стандартными дозами парацетамола с регистрацией в дневнике пациента; применение других препаратов, которые могли бы повлиять на герпес-зостерную инфекцию перед началом или во время исследования, являлось критерием исключения. В окончательный анализ были включены 90 пациентов, из которых 44 получали энзимотерапию (группа Э) и 46 — лечение АЦ (группа АЦ). Обе группы были сопоставимы по антропометрическим и анамнестическим данным. Все участники были иммунокомпетентными, и диагноз ОГ во всех случаях был подтвержден. Ни у одного из пациентов не было тригеминальной формы ВВЗ-инфекции, а также генерализации процесса. В обеих группах было зарегистрировано по одному случаю новой атаки ОГ в сутки 7. Ключевыми конечными точками оценки эффективности были выбраны интенсивность сегментарной боли в дни 0, 7, 14 и 21, общая интенсивность боли за 14 дней (сумма оценок), длительность боли (количество дней от начала лечения), потребление парацетамола (дни и граммы). Поражения кожи оценивались по длительности существования везикул, дню начала образования корочек и длительности существования поражений кожи. В сутки 0 средняя и сильная боль была более частой в группе Э (36 из 44 пациентов), чем в группе АЦ (31 из 46 пациентов). К 7-му дню наблюдений произошел существенный сдвиг в этом распределении — всего 10 пациентов, получавших энзимы, страдали от сильной и средней боли, тогда как в группе АЦ таких пациентов было 16, однако различие не было статистически достоверным (табл. 94). Суммарная оценка боли за 14 дней в группе Э имела среднее значение 16,1, в АЦ-группе — 15,3. Начиная с 14-го дня, не было болей у 33 из 44 пациентов, получавших энзимы, и у 35 из 46 пациентов в группе АЦ. В проспективном наблюдении в течение 1 года было документировано только по 1 случаю ПЗН в этих группах. В обеих группах использовали парацетамол, однако его потребление было меньше в течение всех трех периодов исследования в энзимной группе по сравнению с АЦ-группой. Статистическая оценка динамики поражений кожи не выявила достоверного различия между группами в отношении длительности существования везикул (р = 0,803, двусторонний тест Логранка). Следует отметить сходное частотное распределение в обеих группах и для длительности существования везикул, для начала образования корок и длительности существования поражений кожи. При оценке дополнительных критериев не было обнаружено разницы между группами ни в отношении глобальной оценки успеха лечения врачом-исследователем, ни в отношении переносимости исследуемых препаратов. Среднее значение оценки врачом-исследователем эффективности лечения по шкале вербальной оценки составило 2,0 балла («хорошо»). Высокий уровень соответствия был достигнут между двумя исследуемыми группами в оценке переносимости лечения. Средняя оценка в случае начальной инъекции была равно 2,0 в группе Э и 2,1 в группе АЦ. Переносимость капсул в сутки 7 показала среднее значение 2,3 балла в энзимной группе и 2,2 в АЦ-группе, переносимость в сутки 14 составила соответственно 2,2 и 2,3 балла. Нежелательные побочные эффекты были зарегистрированы у 4 из 44 пациентов в группе Э (у трех из них побочные эффекты определенно связаны с лечением — острая боль в месте инъекции). В группе, получавшей АЦ, побочные эффекты зарегистрированы у 3 из 46 пациентов, один случай расценен как «определенно связанный с лечением». В настоящем исследовании удалось показать, что при использовании рекомендованных дозировок не было явных различий в эффективности и побочных эффектах между комбинацией ферментов и АЦ у иммунокомпетентных пациентов. Статистическая оценка наиболее клинически важных критериев «интенсивность боли в сутки 7» и «длительность существования везикул» не выявила достоверных различий. Данные о большей чатоте случаев средней и сильной боли в сутки 0 в группе, получавшей препарат Вобэ-Мугос Е, чем в группе, получавшей АЦ, а затем — заметно меньшей в сутки 7 и сходной в сутки 14, подтверждают вывод о том, что эти два препарата были, по крайней мере, одинаково эффективными в отношении параметров боли. Такое же заключение можно сделать и в отношении устойчиво более низкого уровня потребления парацетамола в группе, получавшей ферменты. Поскольку слабые побочные эффекты в двух группах не различались по частоте, исследование четко показывает, что комбинация ферментов в использованных дозировках представляет собой положительное дополнение к палитре доступных терапевтических средств для лечения ОГ. Сходные результаты были получены A. G. Mendoza в рандомизированном двойном слепом исследовании эффективности Вобэ-Мугос E в сравнении с АЦ при ОГ, в котором участвовали 40 пациентов. По основному критерию «боль в сутки 7» было обнаружено статистически достоверное различие (р = 0,0095) в пользу группы, получавшей энзимы, а также по второму основному критерию — «суммарная оценка боли за 7 дней» (р = 0,0427). Исследование P. W. Billigmann, проводившееся с участием 192 пациентов, при сходных условиях подтвердило результаты вышеописанного исследования Kleine М.W. в отношении важнейшего главного критерия — сегментарной боли — и не обнаружило достоверных различий между двумя группами в отношении других, ранее не исследованных кожных изменений, кроме сегментарного покраснения на 14-й день. Успешные результаты лечения, которые привели к преждевременному выходу из испытания (до истечения 14 дней), в группе, получавшей энзимотерапию, были получены у 9 пациентов, в АЦ-группе — только у 6 пациентов. Медикаментозную сопутствующую терапию в энзимной группе назначали 26 раз (дерматологические средства) и 24 раза — анальгетики, при лечении АЦ — 31 и 22 раза соответственно. Средняя продолжительность лечения анальгетиками была одинакова в обеих группах — 12,3 дня. Длительность лечения в обеих группах была идентичной — в среднем 13,5 дней. Данные об изменении исследуемых клинических симптомов представлены в табл. 95. Главный исследуемый критерий — сегментарная боль: при сравнимом исходном уровне не обнаружено статистически достоверных различий ни на 7-й, ни на 14-й день. Показателен почти идентичный ход графиков, отображающих тенденции для обеих форм лечения на протяжении всего исследования (рис. 23) и явное снижение оценок после 3-го дня исследования. Аналогичные результаты получены для второго главного критерия — сегментарное покраснение, но на 14-й день было выявлено статистически достоверное (не подтвержденное клинически) различие в пользу АЦ-группы, которое, однако, не удавалось выявить на 21-й день исследования и по последнему измеренному значению. По всем описательно оценивавшимся дополнительным критериям результаты лечения в обеих группах также были сопоставимыми. По последнему измеренному значению не было выявлено статистически достоверных различий (см. табл. 95). Одинаковая эффективность исследованных препаратов подтверждена также субъективными общими оценками эффективности, которые раздельно давали врачи и пациенты по окончании лечения. Оценка как врачами, так и пациентами эффективности лечения в обеих группах была одинаковой — в среднем 1,6 балла (от «очень хорошо» до «хорошо»). Врачи оценивали переносимость проводимой терапии в группе Э на уровне 1,2 балла (от «очень хорошо» до «хорошо»), в АЦ-группе — 1,4 (от «очень хорошо» до «хорошо») (р = 0,104). Пациенты оценили переносимость энзимов 1,3 балла (от «очень хорошо» до «хорошо»), а АЦ — 1,4 балла (от «очень хорошо» до «хорошо»), различия не достоверны (р = 0,310). Нежелательные явления возникли в группе Э между 2-м и 12-м днями у 5 пациентов (5,2 %), в АЦ-группе — между 1-м и 13-м днями у 13 пациентов (13,5 %). По частоте возникновения побочных эффектов обе группы различались достоверно (р = 0,048) в пользу энзимотерапии. В группе Э у двух пациентов были документированы жалобы на боли в желудке, у одного пациента — диарея, тошнота и ощущение тяжести в желудке. В АЦ-группе 11 пациентов жаловались на проблемы с желудочно-кишечным трактом (диарея, гастрит, позывы к рвоте, рвота, тошнота), у одного пациента была обнаружена аллергическая кожная реакция, еще у одного возникла генерализованная аллергическая экзантема. Нежелательные явления длились в группе пациентов, принимавших Вобэ-Мугос Е, в среднем в течение 4,8 дня, тогда как в группе пациентов, принимавших АЦ, — 8,6 дня. В качестве мер в группе Э у двух пациентов была снижена дневная доза препарата. В АЦ-группе в двух случаях (диарея, генерализованная аллергическая экзантема) лечение было прекращено, в трех случаях было назначено дополнительное симптоматическое лечение. Все нежелательные явления не требовали дополнительного лечения и разрешились благоприятно. 25 больных из энзимной группы и 16 пациентов из АЦ-группы предъявляли жалобу на ПЗН. He было выявлено существенных различий среди групп по интенсивности и частоте возникновения болей. Таким образом, оценивая результаты сравнительного исследования эффективности Вобэ-Мугос E и АЦ в терапии ОГ, можно сделать вывод, что оба препарата в отношении главных и дополнительных критериев обнаружили одинаковую эффективность при хорошей или очень хорошей переносимости. Комбинированный ферментный препарат, однако, вызвал значительно меньше побочных эффектов, чем АЦ. Таким образом, в нескольких исследованиях, проведенных со схожими условиями, Вобэ-Мугос E показал, в целом, такую же эффективность, как и АЦ. Вместе с тем остается открытым вопрос о влиянии препарата СЭТ на частоту и течение ПЗН. В литературе описаны примеры положительного влияния препарата Вобэ-Мугос E на ПЗН при ОГ, в том числе уже представленные выше. Клинические преимущества использования препарата Вобэ-Мугос E в сравнении с АЦ приведены М. Wolf, К. Ransberger (1972); W. Bartsch (1983); D. Benakova (1993); M.-W. Kleine (1994): — доказанное более эффективное воздействие на ПЗН (не проявляется или очень быстро исчезает); — минимальные побочные эффекты; — отсутствие ограничений к приему Вобэ-Мугос у пациентов с заболеваниями печени и почек (за исключением случаев проведения гемодиализа); — возможны комбинации Вобэ-Мугос E с виростатиками (противогерпетические препараты) и другими препаратами. В контролируемом проспективном рандомизированном сравнительном исследовании Т. Luger, сравнивавшем эффективность комбинации Вобэ-Мугос E с АЦ и комбинации преднизолона с АЦ, в качестве основного критерия для статистической оценки было выбрано возникновение ПЗН. В исследование были включены 67 пациентов с Herpes zoster. Из них 34 пациента получали Вобэ-Мугос E (ежедневно 3 раза по 5 таблеток) и АЦ (5 мг/кг массы тела через каждые 8 ч внутривенно), а 33 — преднизолон (с 1-го по 5-й день пациенты получали дополнительно 1 раз в сутки 50 мг преднизолона, на 6-й день — 1 раз в сутки 40 мг, на 7-й день — 1 раз в сутки 30 мг, на 8-й день — 1 раз в сутки 20 мг, на 9-й день — 1 раз в сутки 10 мг и на 10-й день — 1 раз в сутки 5 мг преднизолона) и АЦ (5 мг/кг массы тела через каждые 8 ч внутривенно). Длительность лечения в обеих группах составила 10 дней. Дополнительными критериями оценки эффективности лечения были: наличие сегментарной боли и сегментарного покраснения на 5-й или 10-й день и длительность пузырьковых высыпаний (в днях). Пациенты обеих групп были сопоставимыми в отношении возраста, роста, локализации Herpes zoster и пораженного сегмента. В группе, получавшей ферменты, было меньше пациентов женского пола, при этом средняя масса тела в этой группе также была меньше. Симптом эритемы на момент начала лечения был менее выражен в группе, получавшей ферменты (р = 0,02). В группе, получавшей ферменты, ПЗН возникла у 8 пациентов (23,5 %); в группе, получавшей преднизолон — у 10 пациентов (30,3 %). Различие не было статистически достоверным (точный тест Фишера, р = 0,36). Как в отношении сегментарного покраснения, так и в отношении сегментарной боли различия между группами в конце лечения не были статистически достоверными, тогда как в 5-й день существовал небольшой тренд в пользу группы, получавшей Вобэ-Мугос E (эритема: 5-й день р = 0,06, 10-й день р = 0,43; боли: 5-й день р = 0,06, 10-й день р = 0,34). Это, в целом, согласуется с результатами описанных выше исследований. Пузырьковые высыпания сохранялись в обеих группах также в течение примерно одинакового срока. Эффективность препарата Вобэ-Мугос E в терапии ОГ представлена в табл. 96. Адекватная оценка эффективности полиэнзимной терапии в лечении тяжелого OE невозможна без сравнения эффективности Вобэ-Мугос E с новым поколением виростатиков. Так, G. Gross (2003) исследовал эффективность и переносимость энзимотерапии в сравнении с валацикловиром (ВАЦ). В многоцентровом рандомизированном двойном слепом исследовании с параллельными группами по технологии двойного моделирования приняли участие 160 больных. Первичные критерии эффективности определялись как результат глобального теста по семи характеристикам эффективности: — кумулятивная боль до 14-го дня; — дополнительное применение анальгетиков; — сегментарная боль; — время до полного исчезновения боли и отмены анальгетиков; — день, когда впервые обнаружено улучшение кожи; — глобальная оценка эффективности врачом и больным по шкале из 5 пунктов; — хорошее самочувствие по шкале фон Зерссена (Bf-S), Келлер и Рей. Для индивидуальных критериев при выполнении глобального теста были обнаружены следующие результаты: критерий «время до исчезновения боли» оценен по Манн — Уитни (MW) и показал некоторое превосходство Вобэ-Мугос Е. По показателю «кумулятивная боль» у больных, принимавших энзимы, было небольшое превосходство над группой ВАЦ. По суммарному применению парацетамола (дневник пациентов) было обнаружено даже большее превосходство Вобэ-Мугос Е. По глобальной оценке эффективности врачом на 3-м визите было обнаружено небольшое превосходство Вобэ-Мугос Е. Результат глобального теста (MW) свидетельствовал о несколько более высокой эффективности Вобэ-Мугос Е. По глобальной оценке переносимости лечения врачом и больными отмечалось небольшое превосходство Вобэ-Мугос Е. Анализ неблагоприятных последствий лечения не показал разницы между группами. Таким образом, анализ проведенных исследований позволяет считать терапию ГИ с использованием Вобэ-Мугос E равноэффективной стандартной терапии АЦ, при этом в некоторых исследованиях продемонстрировано более значимое влияние СЭТ на болевой синдром (по балльной оценке и потреблению анальгетиков), сроки улучшения состояния кожи, снижение частоты развития ПЗН. Важно подчеркнуть, что в большинстве работ отмечена хорошая переносимость терапии энзимами при отсутствии значимых побочных эффектов. Вобэ-Мугос E расширяет спектр современных эффективных и безопасных препаратов для лечения пациентов с ОГ. | |
|
| |
| Всего комментариев: 0 | |