11:28 Классификация клинических форм внутриутробной герпетической инфекции | |
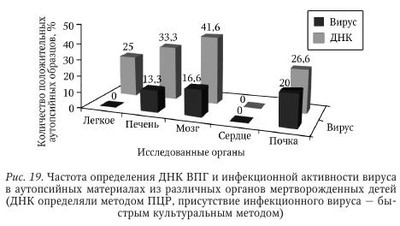
I. Генерализованная (диссеминированная) форма с церебральными и висцеральными повреждениями. И. Локализованная форма: энцефалит, поражение кожи (везикулез), слизистых полости рта, глаз. III. Висцеральная (поражение легких, печени, селезенки, надпочечников). IV. Преимущественное поражение нервной системы: а) транзиторные неврологические изменения, кистозные полости в белом веществе лобных и теменных долей, субэпендимальные кисты; б) ограниченный энцефалит (внутриутробный): в) генерализованная инфекция с менингоэнцефалитом. Установлено, что инфицирование в I триместре беременности приводит к развитию у плода микро-, гидроцефалии, пороков сердца, желудочно-кишечного тракта (ЖКТ), мочеполовой системы, скелета, катаракты, глухоты. Инфицирование во II и III триместрах вызывает у плода гепатоспленомегалию, анемию, желтуху, гипотрофию, пневмонию, менингоэнцефалит, сепсис. Необходимо подчеркнуть, что сепсис у плода чаще является причиной его антенатальной гибели. Восходящий путь инфицирования (из шейки матки) сопровождается размножением и накоплением возбудителя в околоплодных водах и имеет клинические проявления в виде многоводия, невынашивания беременности, задержки внутриутробного развития, отечного синдрома и пр. Ho поражение плода чаще имеет менее тяжелый характер, чем при трансплацентарной передаче инфекции. Показано, что среди беременных женщин, серопозитивных к ВПГ-2, частота угрозы прерывания беременности в 5 раз выше, а многоводие — в 10 раз чаще по сравнению с показателями в группе серонегативных женщин. Невынашивание беременности (ранние и поздние выкидыши, неразвившаяся беременность) отмечаются у 29 % беременных, серопозитивных к ВПГ-2. Среди осложнений родового акта установлен высокий процент несвоевременного излития околоплодных вод. Имеются сведения, что при невынашивании беременности и наличии воспалительных изменений придатков матки ГИ выявляется в 4—8 раз чаще, чем в контрольной группе. Инфицирование может произойти и интранатально, особенно при наличии ГГ у матери. Нужно отметить, что у 70 % матерей, дети которых родились с генерализованным внутриутробным герпесом, в период родов не было признаков ГГ, а у 52 % он не отмечался даже в анамнезе. Однако во время беременности 31 % этих женщин или их мужья имели клинические проявления генитального или кожного герпеса. Наряду с этим возможно постнатальное инфицирование детей при наличии герпетических проявлений на коже, причем не только у матери, но и у других родных или медперсонала. Именно по этой причине акушерки с герпетическими высыпаниями должны отстраняться от обслуживания беременных, рожениц и новорожденных детей до разрешения у больных герпетической сыпи, а дети с ГИ должны быть изолированы в яслях от других детей. Отечественные исследователи продолжают работы по оценке вклада ВПГ-инфекции в развитие ВУИ у недоношенных новорожденных детей. Для этого были изучены клинические образцы от 108 преждевременно родившихся детей (гестационный срок 27,4 + 8,6 нед.) с клиническими признаками ВУИ. Контрольную группу составили 50 здоровых новорожденных детей (гестационный срок 38,2 + 2,3 нед.). Использовали комплекс лабораторных методов: рутинные и специальные серологические методы, БКМ, стандартная ПЦР и ПЦР-РВ. Было установлено, что на первой неделе жизни маркеры ВПГ в группе недоношенных детей обнаруживались чаще, чем в группе доношенных новорожденных детей без признаков ВУИ: 37,5 % против 16 % (р = 0,017). Изучение 561 клинического образца (232 мочи, 197 крови, 59 ликвора, 73 слюны) показало, что ВПГ достоверно чаще выявлялся в моче по сравнению с другими материалами. Использование количественных вариантов BKM и ПЦР свидетельствовало о низкой вирусной нагрузке в организме недоношенных новорожденных детей с ВУИ при первичном обследовании на первой неделе жизни. У большинства недоношенных детей (91,4 %) были обнаружены антитела к ВПГ класса IgG, ни у одного ребенка антител класса IgM обнаружено не было. У 9,4 % серопозитивных недоношенных детей антитела к ВПГ были низкоавидными. В группе здоровых доношенных детей все имели высокоавидные антитела класса IgG к ВПГ. Отсутствие анти-ВПГ или присутствие низкоавидных антител является фактором риска для заражения или развития ВПГ-инфекции. Наиболее важными и показательными были результаты оценки летальности. Так, в группе обследованных недоношенных новорожденных детей с ВУИ среди тех детей, которые имели маркеры ВПГ при рождении, летальность была более чем в 2 раза выше, чем у детей в этой же группе, но не имевших ВПГ. К неблагоприятным исходам беременности помимо преждевременных родов относятся спонтанные аборты, невынашивание беременности, мертворождения. Связь этих явлений с ГВИ давно интересует исследователей. Изучая этиопатогенез спонтанных абортов, обследовали 150 женщин, обратившихся в клинику с гинекологическими проблемами. У 46 % женщин с эрозией шейки матки выявили ВПГ-2, при этом обнаружили ассоциацию между присутствием ВПГ-2 и предшествующим абортом. К аналогичному выводу о корреляции между ВПГ-2-инфекцией и историей спонтанных абортов пришли S. Е. Msuya, проводившие опрос и анкетирование 382 женщин, среди которых у 39 % были обнаружены антитела к ВПГ-2. Риск аборта и преждевременных родов у женщин, инфицированных ВПГ, по оценке отечественных специалистов, соответственно в 1,8 и в 3,2 раз выше, чем у неинфицированных женщин контрольной группы. Изучая ВПГ-инфекцию у 45 беременных женщин в первом и во втором триместрах беременности, авторы использовали тест микронейтрализации анти-ВПГ-2 антител и иммунофлюоресцентный анализ вагинальных и цервикальных материалов. Они установили, что у тех женщин, у которых был один или больше абортов, антитела к ВПГ-2 обнаружены в 64 % случаев, тогда как у беременных женщин контрольной группы — только в 5 % случаев. На основании имеющихся данных Т. Б. Семенова и соавт. заключают, что ГB вызывают до 30 % спонтанных абортов на ранних сроках беременности и свыше 50 % поздних выкидышей. Патологоанатомические исследования плодов и умерших новорожденных часто не позволяют установить этиологию врожденной инфекции. Современные молекулярно-биологические методы, как правило, не используются в практическом здравоохранении для установления посмертного диагноза. Для изучения роли ГВИ в случаях гибели плода, мертворождения, неонатальной и младенческой смерти было проведено комплексное вирусологическое и молекулярно-биологическое исследование. Исследовано 252 органа от 88 умерших новорожденных детей и детей, умерших на первом году жизни, а также 104 органа от 34 мертворожденных детей. Объектами исследования являлись отпечатки органов и лизаты тканей аутопсий. ВПГ выявляли с помощью РИФ, стандартной ПЦР, БКМ, а также с использованием ПЦР in situ. Модификация этого метода была специально разработана для диагностики ГВИ. ПЦР in situ проводили на отпечатках органов в цитологическом препарате. Частота выявления ВПГ в аутопсийных материалах у детей, умерших в течение первого года жизни, составила 18 % по данным БКМ и 20 % — по данным ПЦР. Приблизительно такая же частота выявления ВПГ была установлена в материалах от мертворожденных детей. Максимальная эффективность обнаружения ВПГ в аутопсийных материалах была получена при использовании ПЦР in situ (24 %), минимальная (13,4 %) — с помощью БКМ. Метод БКМ, хорошо зарекомендовавший себя при анализе образцов мочи, слюны, бронхоальвеолярного лаважа и крови от новорожденных детей, оказался значительно менее чувствительным при изучении аутопсийных образцов, что может быть связано с относительно более длительным хранением образцов до исследования и потерей инфекционной активности вируса, сохранение которой необходимо для заражения чувствительных клеток культуры при постановке культурального метода. ДНК ГВ обнаруживали практически во всех исследованных органах (рис. 19). Анализ количества инфицированных клеток в препаратах показал, что наиболее интенсивно накопление ДНК ГВ происходит в тканях мозга и почек (рис. 20, см. цв. вклейку). Следует отметить, что одновременная детекция ЦМВ и ВПГ у мертворожденных и детей, умерших на первом году жизни, показала значительные различия: смешанная ГВИ была определена у 45,4 % мертворожденных детей и у 86 % детей, умерших на первом году жизни (р = 0,01). Сходные данные получены и другими авторами, которые сообщают о том, что частота выявления маркеров ГВ в материалах аутопсии достигает 80 %. Столь высокий уровень ГВ в материалах аутопсии кажется парадоксальным: в России ГВ инфицировано 70—90 % населения, и теоретически группа риска по инфицированию плода не может превышать 10—12 %. Однако полученные результаты могут быть следствием, по крайней мере, трех причин. Во-первых, анализ анамнестических данных матерей мертворожденных показал, что у 1/3 женщин были неоднократные рецидивы ГИ до беременности, а во время беременности они перенесли острые респираторные заболевания, которые могли спровоцировать обострение ГИ и инфицировать плод. Во-вторых, во время беременности наблюдается снижение функционирования некоторых звеньев иммунитета, и при несостоятельности плацентарного барьера уровень антител, способных нейтрализовать вирус, может быть недостаточным. В-третьих, следует учесть, что острые инфекционные заболевания (менингит, энцефалит, миокардит, гепатит, нефрит, панкреатит, интерстициальная пневмония) выявляются значительно чаще у недоношенных плодов и умерших новорожденных по сравнению с доношенными (22,1 % и 3,4 %; р < 0,001), и именно острое инфекционное заболевание в большинстве случаев является непосредственной причиной антенатальной асфиксии плода, преждевременных родов. Таким образом, можно сделать следующие выводы: 1. ВПГ-инфекция, как и инфекции иной этиологии, играет существенную роль в перинатальной патологии, а также в смерти плода и новорожденного. 2. ПЦР in situ — информативный и точный метод, открывающий новые возможности в диагностике ГВИ и позволяющий оценить относительное количество внутриклеточной ДНК и тропность вируса к определенным тканям. Метод эффективен в изучении патогенеза инфекций, вызываемых ЦМВ и ВПГ при фетоинфантильных потерях и летальных врожденных дефектах развития. Этиологическая роль выявленных ГВ подтверждается наличием альтернативно-продуктивных, фиброзно-склеротических изменений в тканях, гигантоклеточным метаморфозом. Верификация инфекционных агентов при мертворождении, врожденных летальных дефектах развития способствует адекватной реабилитационной терапии женщин с потерей плода в анамнезе и прогнозированию исходов будущих беременностей. 3. Выявление ДНК и инфекционно активного ВПГ в клетках и тканях плодов и мертворожденных детей, имеющих различные эмбриофетопатии, дает основание полагать, что инфицирование ВПГ может происходить не только во время родов, но и на стадиях эмбрио- и фетогенеза. | |
|
| |
| Всего комментариев: 0 | |